L'Ema si pronuncerà giovedì 18 su AstraZeneca
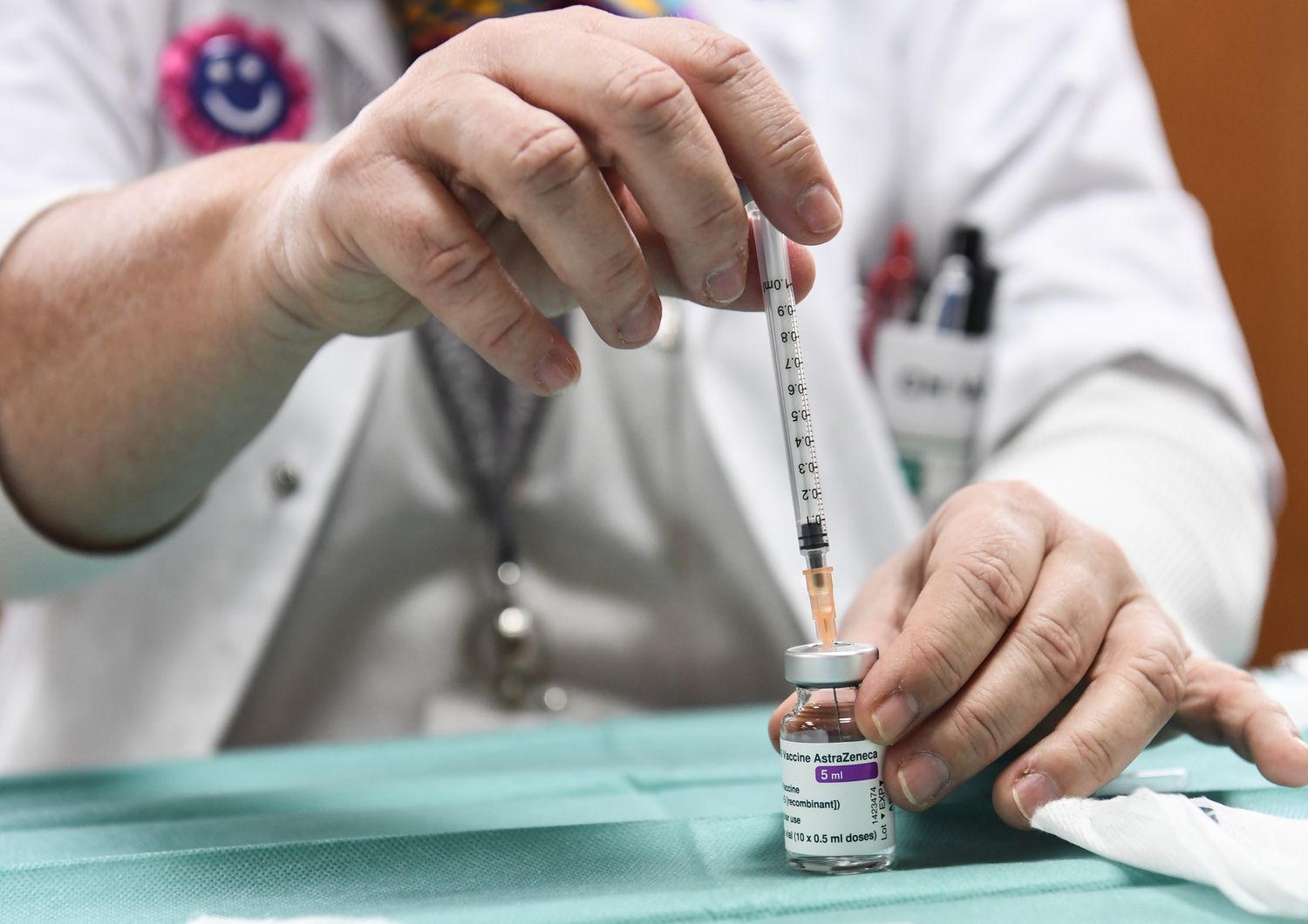

AGI - L'ultima parola su AstraZeneca è attesa per giovedì 18 marzo quando si riunirà in via straordinaria il Comitato dell'Ema per la sicurezza (Prac) che in queste ore è impegnato in una frenetica corsa contro il tempo per analizzare il più grande numero di dati e dare un parere sui casi di trombosi segnalati come possibili effetti collaterali della vaccinazione.
"Diverse autorità responsabili delle campagne vaccinali nazionali nei Paesi dell'Ue hanno temporaneamente sospeso la vaccinazione con il vaccino Covid-19 AstraZeneca. Questa è una precauzione presa alla luce della loro situazione nazionale mentre l'Ema indaga su una serie di eventi di coaguli di sangue in persone che avevano ricevuto il vaccino, come riportato in precedenza", ha spiegato l'Agenzia europea per i medicinali.
"Eventi che coinvolgono coaguli di sangue, alcuni con caratteristiche insolite come un basso numero di piastrine, si sono verificati in un numero molto limitato di persone che hanno ricevuto il vaccino. Molte migliaia di persone sviluppano coaguli di sangue ogni anno nell'Ue per diversi motivi. Il numero di eventi tromboembolici complessivi nelle persone vaccinate non sembra essere superiore a quello osservato nella popolazione generale", ha sottolineato.
L'Ema sta lavorando "a stretto contatto con l'azienda, con esperti in malattie del sangue e con altre autorità sanitarie, tra cui l'Mhra del Regno Unito, sulla base della sua esperienza con circa 11 milioni di dosi somministrate del vaccino". L'indagine dell'Ema "è proseguita nel fine settimana e nei prossimi giorni verrà condotta un'analisi rigorosa di tutti i dati relativi agli eventi tromboembolici. Gli esperti stanno esaminando in dettaglio tutti i dati disponibili e le circostanze cliniche che riguardano casi specifici per determinare se il vaccino potrebbe aver contribuito o se è probabile che l'evento sia stato dovuto ad altre cause".
Il comitato per la sicurezza dell'Ema (Prac) esaminerà ulteriormente le informazioni mercoledì e ha convocato una riunione straordinaria giovedì 18 marzo per concludere le informazioni raccolte e qualsiasi ulteriore azione che potrebbe essere necessaria. La revisione degli eventi tromboembolici con il vaccino AstraZeneca è in corso nel contesto di una segnalazione di sicurezza, con un calendario accelerato.
La segnalazione di sicurezza è un'informazione su un evento avverso nuovo o non completamente documentato che è potenzialmente causato da un medicinale e che richiede ulteriori indagini. La revisione è condotta dal Comitato per la valutazione dei rischi per la farmacovigilanza (Prac), il comitato responsabile della valutazione delle questioni di sicurezza per i medicinali per uso umano. Una volta completata la revisione, il Prac formulerà tutte le raccomandazioni necessarie per ridurre al minimo i rischi e proteggere la salute dei pazienti.